SINTESIS DAN KARAKTERISASI MAGNETIK ENERGI TINGGI DENGAN BANTUAN ULTRASONIK
LAPORAN PRAKTIKUM
KIMIA ANORGANIK
Disusun Oleh
1. Nadya
Arsita
(4311417037)
2. Monica
Avissa
(4311417059)
3. Tri
Maryani
(4311417046)
4. Annisa
Maulidina F (4311417069)
5. Yoga
Samsudianto (4311417068)
JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS NEGERI SEMARANG
2019
SINTESIS DAN KARAKTERISASI MAGNETIK ENERGI TINGGI
DENGAN BANTUAN ULTRASONIK
A. TUJUAN
1.
Mengetahui prinsip kerja sintesis
magnetik energi tinggi dengan bantuan ultrasonik.
2.
Mengetahui karkterisasi sintesis
magnetik energi tinggi dengan bantuan ultrasonik.
B.
LANDASAN TEORI
Magnetit adalah suatu besi
oksida yang memiliki struktur spinel terbalik dengan Fe (III) ion didistribusikan
secara acak antara oktahedral dan tetrahedral situs, dan ion Fe (II) di situs
oktahedral. Keuntungan menggunakan magnetic adsorbent adalah magnetik adsorben
tidak beracun dan dapat digunakan kembali dan mudah dipisahkan dari solusi oleh
magnet eksternal. Untuk sebagian besar aplikasi magnetit, perlu magnetit partikel
nano menjadi seragam ukuran, bentuk dan tersebar dengan baik dalam pelarut (Sulistyaningsih,dkk.2017)
Magnetit nano adalah sejenis
nanomaterial fungsional magnetik, dan memiliki kubik struktur spinel terbalik
dengan oksigen membentuk pengepakan tertutup fcc dan kation Fe menempati
pengantarasitus tetrahedral dan situs oktahedral. Elektron dapat melompati ion
Fe2 + dan Fe3 + di dalam situs oktahedral pada suhu kamar; oleh karena itu, ini
adalah kelas penting dari bahan spintronics. Nanopartikel magnetit memiliki
sifat fisiokimia, magnetik, dan optik yang unik karena permukaan efek dan efek
ukuran terbatas. Nanopartikel magnetit yang menjanjikan ini telah banyak
digunakan sebagai peredam radiasi gelombang mikro, perangkat berbasis spin,
bahan katoda baterai lithium, ferrofluid, penargetan obat dan pembawa pemisahan
sel (Wang,dkk.2013).
Selama beberapa dekade
terakhir, teknik sintesis dari nanopartikel magnetit dan besi oksida milikiselalu
menjadi minat ilmiah dan teknologi. Metode-metode ini termasuk presipitasi
kimia, dekomposisi termal, mikroemulsi, Sol-Gel dan metode oksidasi dari presipitasi.
Namun, sifat fisik dan kimia seragam dari nanopartikel magnetit sangat
bergantung pada rute sintesis, dan bagaimana mengembangkan cara yang sederhana
dan efektif untukmensintesis partikel magnetit dengan dispersi tinggi. Sebagai
contoh, presipitasi kimiawi menyediakan bola bentuk dengan ukuran partikel di
bawah 25 nm. Sebaliknya, ukuran partikel lebih besar dari 50 nm dengan
morfologi cubo-oktahedral diperoleh dengan metode hidrolisis. Selanjutnya
permukaannya modifikasi nanopartikel magnetit dapat meningkatkan tidak hanya
mereka stabilitas dalam pelarut tetapi juga mempengaruhi sifat antarmuka dan
mencegah agregasi antar partikel (Petcharoen.2012).
C.
ALAT DAN BAHAN
1.
Alat :
a.
Gelas
kimia 100 ml
b.
Kertas
saring whatman 0,42
c.
Pengaduk
kaca
d.
Pipet
tetes
e.
Gelas
arloji
f.
Spatula
g.
Pipet
volume 10 ml
h.
Pipet
volume 50 ml
i.
Labu ukur
100 ml
j.
Labu ukur
10 ml
k.
Erlenmeyer
250 ml
l.
Corong
kaca
m.
Probe
Ultrasonik
n.
Neraca
analitik
o.
Oven
p.
Alat FTIR
q.
Alat PSA
2.
Bahan :
a.
Larutan NH4OH
25% 97ml
b.
Akuades
108 ml
c.
FeCl3
. 6H2O 2,98 gram
d.
FeSO4
. 6H2O 1,53 gram
e.
1,2,4-Triazole
0,1 gram
D.
CARA KERJA
1. Preparasi
Larutan
2. Sintesis Magnetit Energi Tinggi Dengan Ultrasonik
F. ANALISIS DATA
G. PEMBAHASAN
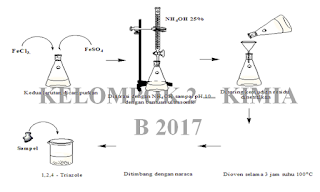
Pada percobaan ini bertujuan untuk mengetahui prinsip kerja sintesis magnetik energi tinggi dengan bantuan ultrasonik dan mengetahui karkterisasi sintesis magnetik energi tinggi dengan bantuan ultrasonik. Menurut Shishehbore (2011) metode yang digunakan pada praktikum ini yaitu kopresipitasi, yang mana dapat dilakukan dengan mencampurkan larutan NH4OH 25% pada campuran larutan FeCl3 dan larutan FeSO4. Metode kopresipitasi merupakan metode sintesis yang paling sederhana, mudah dan tidak membutuhkan temperature yang tinggi, namun dapat menghasilkan partikel Fe3O4 dalam orde nanometer. Pada larutan FeCl3 dan larutan FeSO4 mengandung ion Fe2+ dan Fe3+ yang nantinya ion-ion ini akan mengalami proses kopresipitasi yaitu larutan yang akan mempermudah pembentukan endapan setelah dilakukan penambahan basa yaitu dengan larutan NH4OH, larutan ini berfungsi untuk pembentukan Fe(OH)2 dan Fe(OH)3. Adapun fungsi digunakannya gelombang ultrasonik pada sintesis ini dimaksudkan untuk memperoleh partikel yang lebih homogen dan lebih kecil. Penambahan NH4OH 25% dilakukan tetes demi tetes dengan bantuan buret sampai membentuk endapan mencapai pH 10 didalam lemari asam karena NH4OH 25% bersifat volatil (mudah menguap). Endapan oksida besi yang dihasilkan berwarna hitam pekat, yang mengindikasikan terbentuknya nanopartikel oksida besi Fe3O4. Selain berwarna hitam, endapan ini juga merupakan partikel magnetik. Pada sintesis nanopartikel oksida besi dengan menggunakan metode kopresipitasi, pH larutan memiliki peranan penting dalam menumbuhkan partikel Fe3O4 dan membentuk medium basa (alkali) yang sesuai utuk menghasilkan nanopartikel oksida besi dengan ukuran dan morfologi tertentu (Permana,dkk,2017).
Grafik diatas menjelaskan mengenai perbandingan analisis magnetit dengan FTIR tanpa penambahan 1, 2, 4 – Triazole dan dengan penambahan 1, 2, 4 – Triazole. Pada grafik 1 yaitu analisis magnetit dengan FTIR tanpa penambahan 1, 2, 4 – Triazole menjelaskan bahwa terdapat 4 puncak, puncak pertama berada pada panjang gelombang antara 3388 cm-1 yang menunjukkan magnetit tersebut mengandung uluran O-H. Puncak kedua berada pada panjang gelombang 1628 cm-1 menunjukkan magnetit mengandung O-H. Puncak ketiga berada pada panjang gelombang 892 cm-1 menunjukkan magnetit mengandun N≡O. Puncak keempat berada pada panjang gelombang 588 cm-1 yang menunjukkan puncak magnetit.
Pada grafik 2 yaitu analisis magnetit dengan FTIR dengan penambahan 1, 2, 4 – Triazole menjelaskan bahwa terdapat 4 puncak yang hampir sama dengan analisis magnetit dengan FTIR tanpa penambahan 1, 2, 4 – Triazole. Puncak pertama berada pada bilangan gelombang 3397,24 cm-1 yang menunjukkan bahwa magentit mengandung uluran O-H. Puncak kedua berada pada bilangan gelombang 1627,95 cm-1 menunjukkan magnetit mengandung O-H. Puncak ketiga berada pada bilangan gelombang 892,36 cm-1 menunjukkan magnetit mengandung N≡O. Puncak keempat berada pada bilangan gelombang 587,72 cm-1 yang menunjukkan puncak magnetit. Akan tetapi, perbedaannya terletak pada persen transmitansi (%T), terdapat perbedaan pada puncak ketiga yaitu N≡O dimana analisis FTIR dengan menggunakan 1, 2, 4 – Triazole memiliki puncak yang lebih tinggi dibanding tanpa penambahan 1, 2, 4 – Triazole. Hal ini membuktikan bahwa aplikasi dengan 1, 2, 4 – Triazole berhasil terbentuk.
Karakterisasi magnetit dengan PSA, yaitu sampel ditimbang sebanyak 5 mg lalu dilarukan dalam 10 ml larutan Asam Sitrat 0,1 M sebagai pendispersi kemudian dihomogekan dengan bantuan probe ultrasonik selama 10 menit untuk menghomogenkan dan larutan berubah menjadi coklat pudar. Kemudian larutan tersebut dimasukkan ke dalam kuvet untuk selanjutnya dianalisi menggunakan PSA. Hasil dari analisis menggunakan PSA didapatkan ukuran partikel dan PI magnetit. Metode yang digunakan adalah polynano dan didapatkan ukuran partikel magnetit sebesar 1520,3 nm dan PI sebesar 0,820.
H. SIMPULAN
1
Sintesis
magnetit Fe3O4 dengan metode kopresipitasi yaitu
pengendapan menggunakan larutan basa NH4OH yang menghasilkan
endapan magnetit. Endapan magnetit dipanaskan sehingga terbentuk
serbuk magnetit ekstrak pasir besi yang menghasilkan mineral magnetit
serbuk berorde nanometer.
Berdasarkan hasil sintesis didapatkan magnetit sebesar 1,8430 gram.
2
Karakterisasi
magnetit menggunakan FTIR dan PSA. Untuk karakterisasi PSA didapatkan ukuran
partikel magnetit sebesar 1300 nm dan PI sebesar 0,86.
I. SARAN
1. Sebelum memulai praktikum, mempersiapkan alat dan bahan yang dibutuhkan.
2. Sebelum praktikum sebaikanya dipastikan bahwa memori Hp atau kamera tidak penuh.
3. Saat melakukan video dilakukan hati – hati agar tidak ada perubahan yang terlewat.
4. Sebelum dan setelah praktikum selalu manjaga kebersihan laboratorium.
DAFTAR PUSTAKA
Permana,B;T. Saragi; M. Saputri; . Safriani; I. Rahayu Dan Risdiana. 2017.Sintesis Nanopartikel Magnetik dengan Metode Kopresipitasi. Jurnal Material Dan Energi Indonesia. Volume 7(2) :17 – 20.
Petcharoena, A. Sirivat. 2012. Synthesis And Characterization Of Magnetite Nanoparticles Via The Chemical Co-Precipitation Method. Materials Science and Engineering. Volume 177(B) : 421– 427.
Sulistyaningsih, Triastuti, Sri Juari Santosa, Dwi Siswanta, and Bambang Rusdiarso. 2017. Synthesis and Characterization of Magnetites Obtained from Mechanically and Sonochemically Assissted Co-precipitation and Reverse Co-precipitation Methods. International Journal of Materials,Mechanics and Manufacturing. Volume 5(1) :1-4.
Wang, Benyang, Qifeng Wei , Shiliang Qu1. 2013. Synthesis and Characterization of Uniform and Crystalline Magnetite Nanoparticles via Oxidation-precipitation and Modified co-precipitation Methods. Int. J. Electrochem Science. Volume 8 : 3786 – 3793.
LAMPIRAN
gambar 1. campuran larutan
gambar 3. titrasi sampai pH 10
gambar 4. hasil titrasi di saring
gambar 5. hasil sintesis
gambar 6. karakterisasi triazole
















Komentar
Posting Komentar